That’s why understanding ¿Dónde se sintetizan las proteínas? Es fundamental para el progreso de la ciencia biomédica.
En este artículo, exploraremos los mecanismos celulares de la síntesis de proteínas y sus funciones. También analizaremos el papel importante que desempeñan los biorreactores y fermentadores en la producción de proteínas en los procesos biotecnológicos. Vamos a ello...
Los fundamentos de la síntesis de proteínas
La síntesis de proteínas es un proceso biológico complejo en el que las células producen proteínas, las macromoléculas que hacen casi todo en la célula, desde la actividad enzimática y la estructura hasta la señalización y las respuestas inmunitarias. La síntesis de proteínas se basa en la información genética del ADN. Este proceso tiene dos etapas principales:
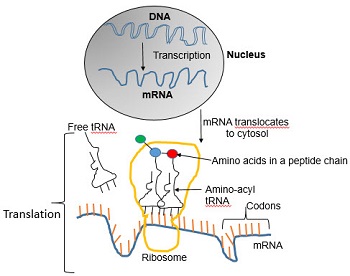
- Stage 1 – Transcription: El ADN se convierte primero en ARN mensajero (ARNm) a través de la transcripción. Esto ocurre en el núcleo de las células eucariotas y en el citoplasma de las procariotas. La ARN polimerasa reconoce el promotor del ADN, extrae el ADN y produce ARNm. El ARNm se edita y se envía al citoplasma para su traducción.
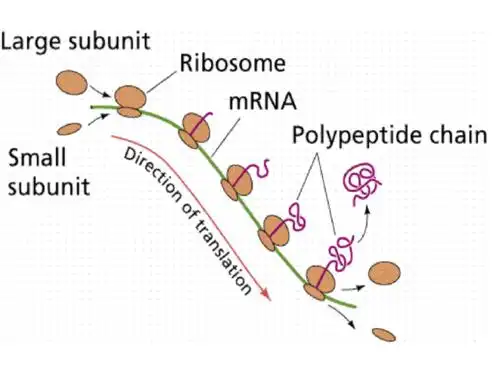
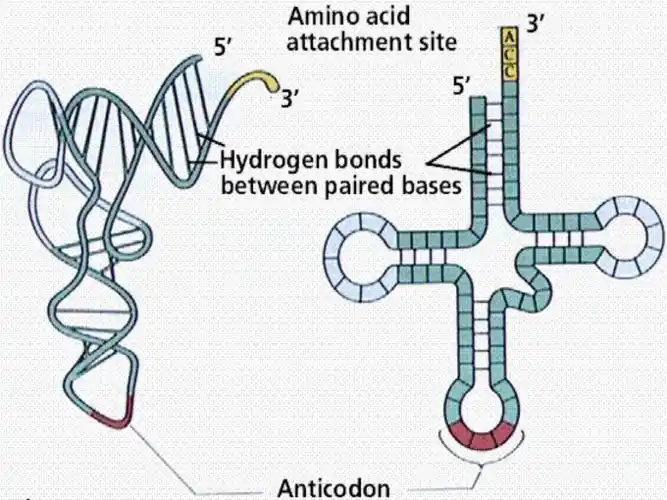
- Stage 2 – Translation: La traducción se lleva a cabo en el citoplasma, donde se ensamblan las proteínas. Los ribosomas leen el ARNm codón por codón en busca de aminoácidos. El ARN de transferencia (ARNt) transporta los aminoácidos correctos que se unen para formar una cadena polipeptídica y se enrollan en una proteína funcional.
¿Dónde se sintetizan las proteínas en la célula?
La síntesis de proteínas se produce en varios lugares clave dentro de la célula, entre ellos: el ribosoma, el retículo endoplasmático rugoso (RE) y el citoplasma. Todas estas estructuras celulares tienen funciones únicas en la síntesis y descomposición de proteínas y, por lo tanto, brindan información sobre cómo las células pueden generar y controlar dichas moléculas.
1) Ribosomas
Los ribosomas son responsables de la síntesis de proteínas tanto en células procariotas como eucariotas. Tienen dos partes principales, la subunidad grande y la subunidad pequeña. Estas subunidades están presentes como estructuras separadas cuando el ribosoma no está funcionando activamente, pero se combinan durante la traducción, que es el proceso de síntesis de proteínas cuando los aminoácidos se unen para formar polipéptidos.
- Ribosomas procariotas:En las células procariotas (bacterias) los ribosomas flotan libremente en el citoplasma para poder responder rápidamente a las necesidades de proteínas de la célula.
- Ribosomas eucariotas: Los ribosomas eucariotas pueden flotar libremente en el citoplasma o adherirse al retículo endoplasmático rugoso. Si están adheridos al retículo endoplasmático, participan en la producción de proteínas secretadas o unidas a la membrana.
2) Retículo endoplasmático rugoso (RE)
El retículo endoplasmático rugoso tiene ribosomas envueltos alrededor de su superficie citoplasmática, por lo que es donde se producen las proteínas para su secreción o incorporación a las membranas celulares. Luego, las proteínas producidas en el retículo endoplasmático rugoso se transportan al aparato de Golgi, donde se purifican y procesan.
- Proteínas de membrana: Producidas en el retículo endoplásmico rugoso, participan en mantener la célula unida y en la comunicación con el mundo exterior.
- Proteínas secretoras: Las proteínas llamadas proteínas secretoras (hormonas, enzimas) se producen en el RE rugoso y se liberan de la célula.
El RE rugoso es el centro de producción de proteínas, donde las proteínas se sintetizan y se pliegan por primera vez para tomar forma para su uso en el organismo.
3) Citoplasma
Los ribosomas libres del citoplasma fabrican proteínas que funcionan dentro de la célula, como las enzimas que llevan a cabo reacciones metabólicas. Estas proteínas son internas a la célula y no se liberan de ella.
Función de las proteínas en el citoplasma:
- Enzimas
- Proteínas estructurales
- Proteínas chaperonas
Por tanto, el citoplasma es esencial para la producción de proteínas que sustentan directamente los procesos internos de la célula.
¿Cómo se sintetizan las proteínas en Biotecnología?
En biotecnología, la producción de proteínas en grandes cantidades es crucial para una amplia gama de industrias, incluidas las farmacéuticas, la agricultura y la producción de alimentos. Y una de las formas más comunes de producir proteínas en grandes cantidades es mediante la tecnología del ADN recombinante, que consiste en introducir ADN extraño en las células para producir proteínas que la célula huésped no produce.
¿Qué es la producción de proteínas recombinantes?
La producción de proteínas recombinantes es un proceso de varios pasos que implica:
- Clonación de genes: En primer lugar, hay que encontrar el gen que codifica la proteína que se desea producir. A continuación, se inserta este gen en un plásmido, un pequeño fragmento circular de ADN que puede replicarse independientemente de los cromosomas de la célula huésped. Este plásmido es el vehículo para transportar el gen a la célula huésped.
- Transformación:Una vez que el gen se clona en el plásmido, este se introduce en una célula huésped. Las células huésped pueden ser bacterias (como E. coli), levaduras o células de mamíferos. Una vez dentro de la célula huésped, el gen se expresa y la célula comienza a producir la proteína especificada por el gen insertado.
- Sistemas de expresión: La célula huésped (bacteriana, de levadura o de mamífero) depende de la proteína. Para proteínas simples se utilizan sistemas bacterianos, para proteínas que requieren modificaciones postraduccionales como la glicosilación (adición de moléculas de azúcar a la proteína) se utilizan células de levadura o de mamífero.
Fermentación y síntesis de proteínas
La fermentación es un proceso biológico en el que las células convierten los nutrientes en energía. Es una parte clave de la biotecnología, especialmente en la producción de proteínas a gran escala. Proporciona un entorno controlado para que las células crezcan y sinteticen proteínas, por eso es importante en los productos farmacéuticos, los alimentos y las enzimas industriales.
1) Fermentación microbiana
La fermentación microbiana utiliza bacterias, hongos o levaduras para producir proteínas, a menudo con ingeniería genética.
- Fermentación bacteriana: La Escherichia coli es una opción popular por su rápido crecimiento y alta expresión de proteínas. Es ideal para producir proteínas recombinantes en las que se introducen genes extraños. Los sistemas de E. coli son rentables y escalables.
- Fermentación con levadura: La levadura, especialmente la Saccharomyces cerevisiae, se elige por su capacidad de realizar modificaciones postraduccionales como la glicosilación. Estas modificaciones son importantes para la estabilidad y la funcionalidad de las proteínas terapéuticas. Los sistemas de levadura se utilizan en las industrias farmacéutica, de biocombustibles y alimentaria.
2) Fermentación de células animales
Algunas proteínas son complejas, especialmente las terapéuticas, y requieren la fermentación de células animales. Las células de mamíferos, como las células de ovario de hámster chino (CHO), son ideales para producir proteínas de alta calidad, como anticuerpos monoclonales y enzimas terapéuticas. Las células CHO realizan modificaciones complejas y producen proteínas muy similares a las proteínas humanas, importantes para los tratamientos médicos. En la fermentación de células animales y microbianas, los biorreactores son importantes para optimizar las condiciones con el fin de maximizar el rendimiento proteico y minimizar los subproductos, a fin de garantizar la eficiencia y la escalabilidad.
El papel de los biorreactores en la síntesis de proteínas
Los biorreactores son la clave para optimizar la síntesis de proteínas. Ofrecen un entorno adecuado en el que se pueden manipular el pH, la temperatura, el oxígeno y las concentraciones de nutrientes. Estas son las variables que se deben optimizar para la proteína objetivo y controlar para los subproductos. Por lo tanto, al proporcionar las condiciones adecuadas para las células microbianas o de mamíferos, los biorreactores mejoran el rendimiento proteico y las proteínas de alta calidad en grandes cantidades.
Uno de los componentes importantes de la tecnología de los biorreactores es la indicación y el control de los diferentes factores que influyen en la formación de proteínas. Los biorreactores que se encuentran en funcionamiento hoy en día cuentan con sofisticados sistemas de control mediante los cuales se pueden hacer muy precisos los parámetros de fermentación o de cultivo celular. A continuación se presentan algunos de los sistemas de control utilizados en los biorreactores:
- Control del pH:El pH del medio de fermentación o de cultivo tiene un gran impacto en las enzimas y las células microbianas. Un pH estable garantiza que las reacciones bioquímicas implicadas en la síntesis de proteínas se lleven a cabo de manera eficiente. El control automático del pH agrega ácido o base para mantener el pH óptimo para el crecimiento y la producción de proteínas.
- Control de temperatura: La temperatura es importante para la expresión de proteínas. Cada organismo o tipo de célula tiene un rango de temperatura óptimo para la actividad metabólica. Los biorreactores con sensores de temperatura y sistemas de calentamiento o enfriamiento mantienen la temperatura dentro de este rango para evitar la desnaturalización de las proteínas y maximizar la producción.
- Monitoreo de oxígeno disuelto: El oxígeno es crucial para los organismos aeróbicos, especialmente en procesos en los que el crecimiento celular y la síntesis de proteínas dependen del metabolismo aeróbico. Los biorreactores tienen sondas de oxígeno disuelto que permiten la medición continua de las concentraciones de oxígeno para satisfacer los requisitos de crecimiento de células microbianas o de mamíferos. El sistema de control automatizado controla las tasas de aireación para regular el suministro y la demanda de oxígeno que interfiere con el funcionamiento celular.
¿Qué biorreactores se utilizan en la síntesis de proteínas?
En función de la proteína, la escala y los requisitos, se utilizan distintos biorreactores para la síntesis de proteínas. A continuación, se presentan los tipos más comunes, sus características, ventajas y desafíos:
1. Biorreactores por lotes
Los biorreactores discontinuos son una solución sencilla para la síntesis de proteínas, especialmente para procesos que no requieren un suministro continuo de nutrientes. Se utilizan para la producción a pequeña escala o piloto.
Características:
- Operar en un sistema cerrado con un volumen fijo de nutrientes añadido al inicio.
- Monitorea y controla el pH, el oxígeno y la temperatura durante todo el proceso.
- Al final del ciclo de producción se cosecha todo el cultivo.
Los biorreactores por lotes son rentables y fáciles de usar, buenos para fines de investigación o a pequeña escala, pero no son eficientes para la producción a gran escala, ya que el agotamiento de nutrientes y la acumulación de subproductos con el tiempo pueden limitar el crecimiento celular y el rendimiento proteico.
2. Biorreactores continuos
Otro tipo de biorreactor es el biorreactor continuo, destinado a la producción de proteínas a gran escala. Este tipo de biorreactores es el más adecuado cuando es necesario mantener una producción constante durante largos periodos de tiempo.
Características principales:
- Los nutrientes frescos se introducen continuamente en el reactor mientras que simultáneamente se cosecha el cultivo.
- Se aplican dispositivos de monitoreo avanzados para controlar el nivel de nutrientes y desechos.
- Se integran sistemas de monitoreo avanzados para mantener el equilibrio de nutrientes y desechos.
Los sistemas continuos han demostrado tener una alta productividad y la proteína producida es de calidad uniforme, características que los hacen adecuados para la producción a gran escala, pero requieren un control sofisticado y son vulnerables a cambios en las condiciones de operación, lo que influye en el rendimiento y la calidad del producto.
3. Biorreactores de lotes alimentados
Los biorreactores por lotes alimentados combinan los beneficios de los sistemas por lotes y continuos, lo que los hace versátiles para producir proteínas de alto valor como anticuerpos monoclonales y enzimas.
Características principales:
- Los biorreactores por lotes alimentados son una mezcla de procesos por lotes y continuos que son útiles en la producción de proteínas valiosas como anticuerpos monoclonales y enzimas.
- Previene el agotamiento de nutrientes y la acumulación de subproductos que pueden inhibir el crecimiento celular.
- Permite un control preciso sobre las estrategias de alimentación para optimizar la producción de proteínas.
Debido a su flexibilidad y a los altos rendimientos que ofrecen, pueden utilizarse tanto en laboratorios como en industrias. Sin embargo, requieren un control estricto de las mediciones, la frecuencia de alimentación y el tamaño de las porciones, lo que puede generar una mayor complejidad operativa.

4. Biorreactores de elevación de aire
Los biorreactores de elevación por aire se utilizan para la producción de proteínas a partir de células microbianas o de mamíferos cuando se requieren tasas bajas de esfuerzo cortante. Utilizan flujo de gas para mezclar, no agitación mecánica.
Características principales:
- Utilice inyección de aire o gas para crear circulación interna y transferencia de oxígeno.
- Mezcla suave para líneas celulares o proteínas sensibles.
- Eficiencia energética con mínimas piezas mecánicas.
Los biorreactores de elevación por aire son ideales para aplicaciones que requieren una oxigenación eficiente y un bajo estrés celular, como el cultivo de células de mamíferos para productos biofarmacéuticos. Pero el flujo de gas para la mezcla limita su uso a ciertos tipos de células o proteínas y la ampliación requiere una cuidadosa consideración del diseño.

5. Biorreactores de tanque agitado
Los biorreactores de tanque agitado son los sistemas más utilizados para la producción de proteínas, ofrecen gran flexibilidad y control sobre las condiciones de producción.
Características principales:
- Tienen un impulsor accionado mecánicamente para una mezcla uniforme de nutrientes, gases y células.
- Permite un control preciso de parámetros ambientales como temperatura, pH y oxígeno disuelto.
- Compatible con todas las básculas desde laboratorio hasta producción industrial.
Estos biorreactores son versátiles y adecuados para cultivos de células microbianas y de mamíferos. Mantienen condiciones óptimas para un alto rendimiento y calidad de las proteínas. Sin embargo, las piezas mecánicas pueden introducir tensiones de corte que pueden afectar a las líneas celulares o proteínas sensibles.
Conclusión
La síntesis de proteínas es un proceso celular crítico. Si se conocen mejor sus funciones y se aumenta la eficiencia de producción mediante mejores biorreactores, las industrias alimentaria, farmacéutica y otras pueden satisfacer eficazmente las necesidades mundiales de proteínas. BaiLun Biotechnology Co., Ltd. está liderando el camino al desarrollar biorreactores nuevos y eficientes que abordan por completo las deficiencias actuales de los modelos antiguos.
Los biorreactores de BaiLun Biotechnology Co., Ltd son funcionales, económicos y confiables. Ya sea que se trate de un sistema a escala de laboratorio o de un equipo industrial, BaiLun ofrece soluciones tecnológicas y servicios de consultoría profesional para garantizar su éxito. Póngase en contacto con BaiLun hoy y descubra cómo podemos mejorar sus procesos biotecnológicos.

